
Prof. Jennifer Doudna 2002 yılından beri Kaliforniya Üniversitesi Berkeley’de öğretim üyesi. Kimya ve MCB (Moleküler Hücre Biyolojisi) departmanlarında görevi olan Prof Doudna’nın son zamanlarda gördüğü ilgi yaptığı işin değerine kıyasla az denebilir. Prof. Doudna’nın mekanizmasını çözdüğü ve kullanmayı başardığı Crispr/Cas9 sistemiyle organizmaların DNA’sını bir word belgesi düzenler gibi düzenleyebiliyor, istenilen genler üzerinde kolayca değişiklikler yapılabiliyoruz. Genlerle oynamak deyince hemen akla gelen embriyo halindeyken, istenilen genlerin eklenip çıkarılabileceği “sipariş bebekler” ya da süper insan fikri hala sadece filmlerde görebileceğiniz tarzdan bir ütopya fakat Prof. Doudna ve belli başlı bilim adamlarının tüm dur çağrılarına rağmen insan embriyosu üzerinde de çalışmalara başlayan Çinli bilim adamları şimdilik başarısız olsalar da, sistemin fareler üzerinde olumlu sonuçlar vermesi, ileriki zamanlarda neler olabileceğinin bir göstergesi.
Crispr/Cas9 Nedir, Nasıl Çalışır?
Bakteri DNA’larını inceleyen bilim adamları 1980’lerden beri belli aralıklarla birbirinden ayrılmış ve tekrar eden dizinlere rastlıyorlar. CRISPR (Clustered Regularly Interspaced Palindromic Repeats yani “düzenli aralıklarla bölünmüş palindromik tekrar kümeleri”) denen bu dizinlerin görevi ve nasıl bakteri DNA’sına entegre olduğu kısmen 2005 yılında keşfediliyor. (Son 10-20 yılda biyoloji aldı yürüdü, fizik ve kimya çok daha durağan kaldı, en basit örneklerinden biri belki milyonlarca yıldır bakterilerin kullandığı bu savunma sistemin yeni yeni anlaşılıyor olması.) DNA’daki tekrar eden dizinlerin arasındaki bölümler detaylı incelendiğinde mesele daha da garipleşiyor, çünkü bu DNA parçaları bazı virüslerin DNA’sıyla birebir eşleşiyor. İşin sırrı kendi DNA’sında virüs DNA’sından parçalar taşıyan bakterilerin o virüslere karşı dirençli olduğunun fark edilmesiyle açığa çıkıyor. Şöyle ki bakteriler, saldırısından sağ kurtulmayı başardıkları virüslerin DNA’larından parçaları, kendi DNA’larına ekleyen ve bu sayede aynı virüsün sonraki saldırılarından korunmayı sağlayan bir savunma sistemine sahipler. Hücreye giren her yeni virüsün DNA parçaları Crispr dizilimi içinde kaydediliyor. Böylece bakteri DNA’sında bir envanter listesi çıkartılmış oluyor. Kısacası, bakteriler hücrelerine giren ve kurtulmayı başardığı virüslerin birer kopyasını, adeta “arananlar” listesi şeklinde kendi DNA’sında saklıyor.
Hücrenin saldırılardan kurtulabilmesi için virüs listesine sahip olması tek başına yeterli değil. Bakterinin virüs kontrolü ele almadan DNA’sını tanıması ve parçalaması gerekli. İşte bu aşamada CRISPR’dan sentezlenen RNA’lar (crRNA) ve Cas proteinleri devreye giriyor. crRNA’lar virüs DNAları baz alınarak sentezlenen tek sarmal RNA’lar ve virüs hücreye girdiğinde virüs DNA’sıyla nükleotit eşleşmesi (base pairing) yaparak tanımayı sağlıyor. Cas proteinleri ise birer nükleaz (nuclease) ve çift sarmal DNA’yı kesmekle görevliler. crRNA’lar Cas9’a bağlanıp virüs DNA’sıyla eşleştiklerinden, Cas9 proteini de otomatik olarak virüs DNA’sına bağlanmış oluyor. Sonrasında bu protein bağlanılan yeri çift sarmaldan keserek virüs DNA’sını parçalıyor ve etkisiz hale getiriyor. Yani, virüs DNAsından kopyalar alan bakteriler, o nükleotit dizisini baz alarak sentezledikleri RNA ve proteinlerle hücreye giren virüsleri hedef alıp parçalayan bir savunma mekanizmasına sahipler.
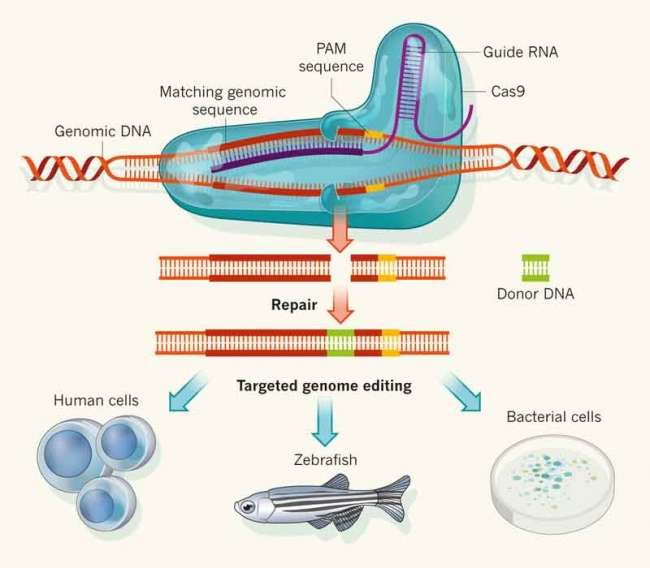
İyi de bakteri kendini kurtarıyor, bize ne faydası var diyebilirsiniz. Bizim işimize yarayan kısmı Cas9’ın hedef DNA’lar üzerinde rastgele değil de, crRNA/rehber RNA’lar sayesinde nokta atışı yerlere bağlanabilmesi. Şöyle ki, virüs DNA’sını hedef almak yerine, bir gen dizilimini kullanarak rehber RNA üretsek, bu sayede Cas9 bizim hedef aldığımız gene bağlanacak. Cas9’ın aktif kısmındaki bir mutasyonla DNA’yı kesme işlevini yapamaz hale getirdiğinizde ise, elinizde DNA üzerine boncuk dizer gibi “bloklar” yerleştirebileceğiniz bir sisteminiz oluyor.
Liseden beri herkes bilir, biyolojinin temel presiplerinden biri “merkezi dogma”dır. DNA’dan RNA, ondan da ribozom sayesinde protein sentezlenir. Fakat bize pek öğretilmeyen (en azından ben öğrendiğimde çok harika bulmuştum) bu işlemleri gerçekleştiren sistemler ve onların çalışma prensipleri. DNA’dan RNA transkripsiyonu, RNA polimeraz denilen yine başka bir protein sayesinde olur. RNA polimeraz, en basit şekliyle, DNA sarmalının tek şeridi üzerinde kayarak ilerler ve RNA sentezler. crRNA sayesinde DNA üzerinde istediğimiz yere yerleştirdiğimiz inaktif Cas9’lar, yol kapanı gibi hareket ederler ve RNA polimerazın DNA üzerinde kaymasını engellerler. Bu şekilde hedef alınan gen için RNA sentezlenememiş olur. Doğal olarak da o gene (ve genin karşılığı RNA’ya) karşılık gelen protein üretilemez. Böylece hedef alınan gen inaktif hale getirilmiş olur.

İstediğimiz genleri inaktif hale getirebilmemiz çok güzel. Bu sistemi farelerde siyah kıl rengine sebep olan proteini/geni inaktif ederek denediler ve fare embriyolarına bu sistemi uyguladılar. Sonuç yandaki fotoğrafta. Fakat esas ulaşılmak istenen nokta, genleri modifiye edebilmek ya da tamamen değiştirebilmek. Daha basit terimlerle anlatmak gerekirse DNA’yı kesip içinden bozuk olduğunu düşündüğünüz parçayı çıkarmak ve/ya yenisini yerleştirmek gerekli. crRNA’larla hedef alınan kısımlar, aktif Cas9 kullarak kesiliyor. Sonrasında hücreye yama etmek istediğiniz DNA parçalarını enjekte ediyorsunuz. Yamanacak parçayı öyle bir ayarlamanız gerekli ki, başı sonu orijinal DNA ile uyuşsun ve hücrenin sahip olduğu DNA tamir enzimleri gelip sanki yama parçası orijinal DNA’daymış ama kopmuş gibi gelip dikebilsin. (Bu yönteme homologous directed repair deniyor.)
Yeni parça dikme işlemi maalesef inaktive etmekten daha zor, çünkü parçaların düzgün eşleşmeme ihtimali ya da kesilen DNA’nın orijinal haliyle yeniden dikilme ihtimali oldukça yüksek. Bununla beraber her iki durum içinde geçerli olan bir hayli limitasyon daha var. crRNA’ların DNA ya bağlanması ne kadar spesifik olsa da, spesifik olmayan ve DNA üzerinde rastgele yerlere de belli oranda bağlanması söz konusu. Dahası sisteminiz düzgün çalışsa bile, gen entegre edilen embriyoların sağlıklı gelişimlerin devam ettirip ettiremeyeceği de şüpheli ve böylesi ciddi bir operasyon sonrası gelişen embriyolarda ne tarz yan etkiler görülebileceği henüz yeterince test edilmiş değil. İnsan gibi kompleks bir organizma üzerinde kullanabilmek için tüm bunlar aşılması gereken sorunlar.
Şimdi bir adım geriye gidip bu sistemi kullanarak varmak istediğimiz noktayı hatırlamakta fayda var. Daha uzun ömür, hastalıklara karşı doğuştan bağışıklık, üstün zekalılık gibi pratik hayaller, genetik ya da biyoloji çalışmalarına yeni başlayanların hep aklında olmuştur. CRISPR-Cas9 sistemi de bu doğrultuda 2 amaca hizmet edecek şekilde kullanılabilir. 1- Düzgün çalışmayan ya da hastalıklara sebep olacak genlerin ve işlevsizleştirmek ve protein sentezini durdurmak. 2- Organizmaya yeni özellikler kazandıracak genler eklemek ya da mevcut genlerin yerine daha sağlıklı, dayanıklı, zeki vb. istenilen özellikteki genleri organizmaya embriyodan olmak üzere yerleştirebilmek.
Doudna lab sentetik rehber RNA’lar üreterek DNA üzerindeki istedikleri yeri hedef alabilen Crispr/Cas9 teknolojisini bakterilerden adapte ettiler ve tüp üzerinde, hücre dışı ortamda bunun yapılabilirliğini ilk kez 2012 yılında gösterdiler. Daha önce kullanılan birçok gen mühendisliği tekniği olmasına rağmen, Prof. Doudna’nın çalışması önceki tekniklere kıyasla uygulaması çok daha kolay ve hücrenin kendi sahip olduğu mekanizmaları işleten bu sistem verimlilik olarak da eski metodlardan çok daha ilerde. İşte bu sebeplerden Prof. Doudna ve çalışması sadece bilim dünyasında değil, insanlığa sunabileceği faydalar nisbetinde her kesim tarafından büyük ilgi görüyor.
Bilimsel problemler ve teknikteki eksiklikler bir yana, bu tarz bir gücün insan emrinde olması birçok etik soruyu da beraberinde getiriyor. İmkanlara sahip insanların çocukları “süper insan” yapılabilirken, zaten gelir dağılımının düzensiz olduğu günümüzde, bir de nesilden nesile aktarılacak genetik değişikliklerle bu uçurumun daha da artması, belki de önlenemez hale gelmesi söz konusu. Elysium filmini izlemeyenler varsa tavsiye ederim, tam da bu problem üzerinde duruyor. Zengin bir kesim insanın harika koşullardaki bir uzay istasyonunda yaşadığı bir gelecekte, darmadağın bir dünyada yaşam mücadelesi veren insanların varlığı konu alınıyor filmde. Eğer insan genetiğiyle oynama kontrol altına alınıp düzgün takibi yapılmazsa, gerçek hayatta böyle senaryolarla karşılaşmak çok da şaşırtıcı olmayabilir. Tabi ki her teknolojik gelişme gibi kim tarafından ve hangi amaçlarla kullanılacağı tüm bunları belirleyecek. Felaket tellalığı yapmaya henüz gerek yok, çünkü sanıyorum ki sistemi memeliler üzerinde hatasız çalışır hale getirmek için daha uzun bir yol var önümüzde.
Not: Bu sistemi en güzel anlatan kişi hiç şüphesiz Jennifer Doudna’nın kendisidir. Prof. Doudna’nın ağzından Crispr Cas9 sistemini dinlemenizi kesinlikle izlenmenizi tavsiye ederim:
Referanslar ve İleri Okuma:
http://www.sciencemag.org/content/337/6096/816.full
http://www.origene.com/crispr-cas9/
http://www.cell.com/nucleus-CRISPR
http://www.sciencemag.org/site/products/collectionbooks/CRISPR-Cas9_booklet_HighRes.pdf
http://www.nytimes.com/2015/05/12/science/jennifer-doudna-crispr-cas9-genetic-engineering.html?_r=1
http://newscenter.berkeley.edu/2014/11/10/jennifer-doudna-saul-perlmutter-named-2015-breakthrough-prize-winners/









![Uzay Çalışmalarının Önemi - Süleyman Fişek [Röportaj] Uzay Çalışmalarının Önemi - Süleyman Fişek [Röportaj]](https://fizikist.com/uploads/img/uzay-calismalarinin-onemi.jpg)




0 yorum